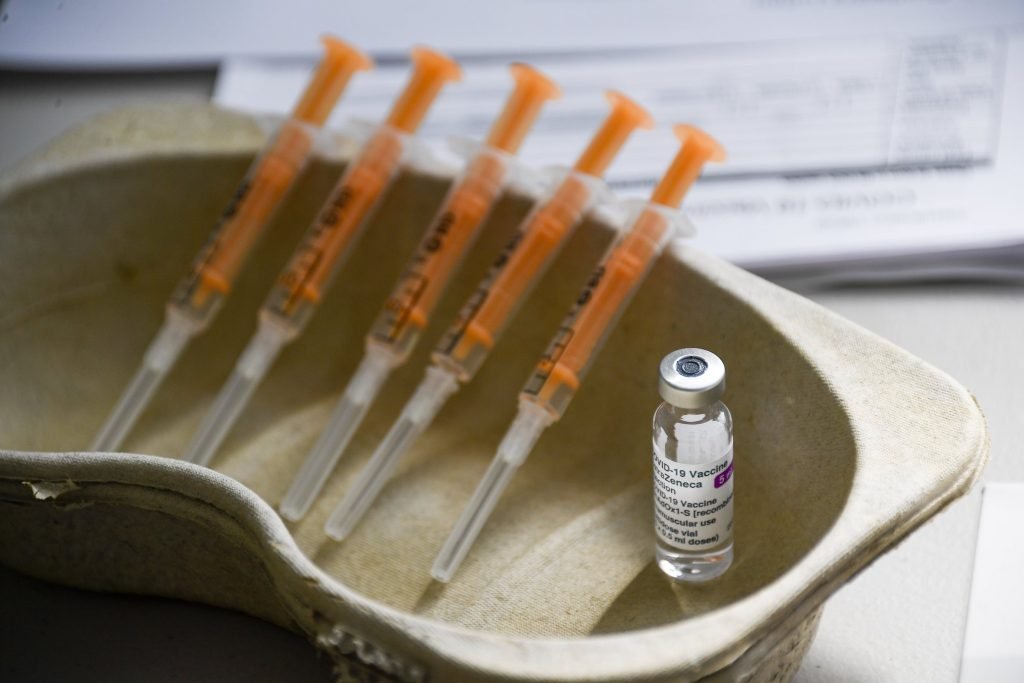
Le vaccin d’AstraZeneca devait sauver le monde de la pandémie: un vaccin peu coûteux, facile à conserver et à administrer qui protégerait non seulement les citoyens des pays riches, mais aussi des plus vulnérables. Un game-changer, titrait la presse anglo-saxonne. Les choses ont tourné différemment. La saga AstraZeneca ressemble de plus en plus à un mauvais feuilleton. Comment en est-on arrivé là?
En fait, le vaccin, fruit d’une collaboration entre des chercheurs de l’Université d’Oxford et l’une des plus grandes sociétés pharmaceutiques du monde, a été en proie à des faux pas depuis le début. Dès le départ, il y a eu beaucoup de confusion sur les résultats des tests de phase 3. Ensuite, c’était au tour des fameuses livraisons retardées. Puis les rapports de caillots sanguins chez une poignée de vaccinés, semant la panique. Enfin, cette semaine, un coup de grâce: les résultats d’une étude sur l’efficacité du vaccin d’AstraZeneca étaient basés sur des données obsolètes.
Pourtant, si l’introduction du vaccin d’AstraZeneca avait été gérée différemment, il aurait pu devenir ce game-changer que l’on nous a vendu. Les pays qui ont utilisé le vaccin à grande échelle, comme la Grande-Bretagne, montrent qu’il provoque une baisse spectaculaire des hospitalisations et des décès. Mais la confiance du public dans le vaccin a pris un gros coup, sapant son acceptation et retardant la lutte contre la pandémie.
Les sondages suggèrent la confiance accordée au vaccin d’AstraZeneca est en baisse. Nulle part les conséquences ne sont plus apparentes qu’en Europe. Une Europe qui a beaucoup misé sur le vaccin d’AstraZeneca, mais qui n’a jusqu’à présent obtenu qu’un tiers des doses qui promises.
Une vague de battage médiatique
Le vaccin d’AstraZeneca a déclenché une vague de battage médiatique au printemps dernier. Un article en première page du New York Times déclarait que le vaccin d’Oxford était en avance sur tout le monde. La scientifique d’Oxford Sarah Gilbert y laissait entendre à l’époque qu’elle était sûre que le vaccin fonctionnerait – avant même qu’une seule personne n’ait bénéficié de la moindre injection dans un essai clinique.
Dès le début, le groupe d’Oxford a diffusé des communiqués de presse dithyrambiques les uns après l’autre, se vantant de la merveilleuse et inaltérable marche en avant. L’équipe qui a développé le vaccin est en ce sens apparue comme arrogante pour de nombreux scientifiques des deux côtés de l’Atlantique.
Adrian Hill, un membre-clé de l’équipe d’Oxford, a toujours défendu cette communication précoce sur le vaccin. ‘Les virologues ont prédit qu’un vaccin contre le coronavirus pourrait être prêt dans les 12 à 18 mois. Nous n’étions pas d’accord. Nous avons dit que nous l’aurions déjà avant septembre. Si c’est vantard, je suis désolé, mais c’était vrai’, a déclaré Hill dans une interview.

Des mois d’avance
Hill et ses collègues considéraient leur travail comme une solution mondiale – pas seulement pour les pays riches. AstraZeneca a d’ailleurs déclaré qu’elle ne cherchait pas de profit. Notamment en fixant le prix à moins de 4 dollars la dose – à peine un cinquième de ce que certains de ses concurrents factureraient. Le vaccin pouvait également être conservé dans des réfrigérateurs ordinaires, contrairement à ceux de Pfizer/BioNTech et de Moderna, ce qui le rend plus faciles à administrer dans les pays en développement aux systèmes de santé fragiles.
En mai, des mois avant que les fabricants rivaux lancent des essais cliniques majeurs, Oxford et AstraZeneca annonçaient qu’ils testeraient leur vaccin sur 10.000 personnes au Royaume-Uni. Peu de temps après, les États-Unis faisaient savoir qu’ils dépenseraient jusqu’à 1,2 milliard de dollars pour que 300 millions de doses soient disponibles dès octobre – il s’agissait initialement de la plus importante commande de vaccins aux États-Unis. Le 13 juin, la Inclusive Vaccine Alliance (Allemagne, France, Italie et Pays-Bas) annonçait un accord portant sur 300 millions, puis 400 millions de doses du vaccin Oxford/AstraZeneca, un accord qui sera élargi à l’ensemble de l’UE en août.
Mais avant que les injections puissent être administrées en Europe et aux États-Unis, le vaccin AstraZeneca devait être testé dans un essai impliquant 30.000 personnes, un choix que les scientifiques ont fait pour s’assurer de l’efficacité du vaccin. Ces essais devaient étudier toutes les tranches d’âge pour ne laisser aucune place au doute.
Confus et contradictoire
Cela ne s’est pas déroulé sans heurts. De rares symptômes neurologiques sont survenus chez trois personnes, suspendant les essais dans le monde entier pour déterminer si cela était lié au vaccin. Aucune preuve d’un lien n’a finalement été trouvée, mais cela a retardé les processus.
Ensuite, certains des participants au programme-pilote britannique ont reçu de manière inattendue une première dose qui n’était que la moitié de celle initialement prévue, et l’explication donnée était assez déroutante: le problème semblait être lié à un sous-traitant italien qui utilisait une technique différente pour mesurer l’ingrédient actif du vaccin. Hill déclarait à l’époque que les chercheurs avaient reçu l’approbation réglementaire pour administrer une dose supplémentaires aux sujets, affirmant même qu’aucune erreur ne s’était produite. ‘C’est perçu comme une erreur, mais c’est en fait une observation scientifique’, justifiait-il.
Ce problème de dosage est devenu plus tard un point de confusion lorsque la société a publié les résultats des tests dans le monde en novembre. Dans le groupe à la demi-dose, l’efficacité du vaccin s’est avérée jusqu’à 90%, contre 62% chez les volontaires qui ont reçu le régime complet à deux doses. Les scientifiques d’Oxford ont admis qu’ils ne pouvaient pas expliquer pourquoi le groupe de dosage non conventionnel avait une protection supérieure.
Par la suite, il est finalement apparu qu’au lieu d’un intervalle de quatre semaines entre les injections, certains participants du groupe de la demi-dose avaient reçu des injections à trois mois d’intervalle, ce qui expliquait cette différence.
Où sont les plus de 65 ans ?
Le plus important peut-être, selon certains scientifiques, est que l’équipe d’AstraZeneca avait finalement décidé de ne pas mettre l’accent sur le recrutement des personnes âgées pour leurs premiers essais cliniques au Royaume-Uni, et aucune conclusion solide n’a donc pu être tirée sur l’efficacité du vaccin sur les plus de 65 ans – le groupe pourtant le plus à risque de maladie grave. En l’absence de données à ce sujet, certains pays européens ont conseillé de ne pas administrer de doses du vaccin aux personnes âgées.
Mais l’Europe a très vite cru aux promesses d’AstraZeneca. Le vaccin est devenu le centre d’une stratégie d’achats collectifs négociée au nom des 450 millions d’habitants de l’UE. La Commission européenne s’est fortement engagée envers AstraZeneca: 300 millions de doses dans un contrat signé mi-août. En fait, les responsables européens s’attendaient à ce que le vaccin d’AstraZeneca soit prêt en premier. Mais alors que l’automne passait à l’hiver – et qu’une deuxième vague plus importante que la première frappait le Vieux Continent – le doute s’immisça: l’Europe avait-elle misé sur le bon cheval ?
La bombe a éclaté
Le vaccin d’AstraZeneca n’a été approuvé dans l’Union européenne que fin janvier, six semaines après le Royaume-Uni, à un moment où une variante plus contagieuse du coronavirus se propageait à travers le continent et grandissait chaque jour. Outre ce retard à l’allumage, Pascal Soriot, PDG d’AstraZeneca, annonça ce qui sera vécu comme un coup de tonnerre: l’UE ne recevrait pas 90 millions de doses à la fin du mois de mars, mais 30 millions. Quelque temps après, rebelote, la société déclarait que la livraison serait également moindre au deuxième trimestre.
Von der Leyen, qui a présidé les négociations sur les vaccins en tant que présidente de la Commission européenne, est attaquée de toutes parts. Des prix négociés au rabais font passer l’UE en dernier dans la file d’attente. On reproche aussi à l’UE de ne pas avoir assez investi dans la recherche de vaccins en 2020. Selon le Financial Times, quand le Royaume-Uni et les États-Unis ont dépensé 28 et 29 livres sterling par habitant, l’Europe n’en a investi que 4. En outre, von der Leyen l’annonce elle-même, l’UE a exporté 77 millions de doses produites sur son territoire, contre 62 millions de doses administrées. L’UE a donc exporté plus de doses qu’elle n’en a administrées, faute de vaccins disponibles. Des chiffres qui passent évidemment très mal, même si l’Europe est contractuellement liée à ces exportations. Il y a de quoi tomber de sa chaise: l’UE a exporté 21 millions de doses vers le Royaume-Uni. Pas une seule n’a fait le chemin inverse depuis les sites de production britanniques.
Tentant de se racheter, Ursula von der Leyen mène depuis un bras de fer contre le Royaume-Uni et AstraZeneca. Les géants pharmaceutiques qui n’assureraient pas leurs livraisons pourraient faire face à des restrictions sur les exportations de vaccins fabriqués sur le Vieux Continent. Or, on sait que l’Europe est un énorme centre de production dont beaucoup de pays dépendent. Un jeu dangereux: de nouveaux acteurs comme Johnson&Johnson – qui a aussi témoigné de probables retards – pourraient prendre peur face aux menaces de l’UE. En outre, un acteur comme Pfizer qui a jusqu’à maintenant assuré ses livraisons se verrait injustement sanctionné ou menacé.
Plusieurs pays dont la Belgique et les Pays-Bas, deux endroits où l’on fabrique beaucoup de vaccins, n’ont pas voulu entrer dans ce bras de fer. Finalement, suite au Sommet européen de jeudi soir, un compromis a été trouvé: l’UE se donne les moyens de limiter les exportations par l’introduction de deux nouveaux critères. Dans les faits, il est peu probable que cela arrive. En témoigne cette déclaration de von der Leyen à la sortie du Sommet: ‘L’UE est fière d’abriter les producteurs de vaccins qui livrent non seulement aux citoyens européens, mais exportent aussi dans le monde entier. Nous veillerons à ce que les Européens reçoivent leur juste part de vaccins et nous continuerons à soutenir la vaccination dans le monde.’ L’Europe défend son image de continent non égoïste et universaliste.
Mais l’Europe payera les pots cassés: selon une étude menée par Euler Hermès, les retards de livraisons coûteront, s’ils ne sont pas rattrapés, la bagatelle de 123 milliards d’euros en 2021 pour les 27 États membres.
Caillots sanguins et signaux contradictoires
Les retards dans les livraisons ne sont qu’une partie du problème. Les dirigeants européens ont eux-mêmes miné la confiance du public dans le vaccin d’AstraZeneca. Début, mars, le Danemark et la Norvège font état d’un problème de caillots sanguins graves ou mortels chez des jeunes ayant reçu le vaccin. Quelques cas sur des millions, mais les régulateurs déclarent que c’était statistiquement significatif et arrêtent les vaccinations pour enquêter et en retirer une éventuelle causalité. L’Allemagne, puis la France, l’Italie, l’Espagne suivent. En tout, plus de 10 pays de l’UE décident de suspendre le vaccin pour quelques jours seulement. La Belgique n’a cette fois pas cédé à la panique générale et a attendu un nouvel avis de l’Autorité européenne des médicaments. Un avis finalement positif , tout comme celui de l’OMS. Mais le mal était fait.

Entre-temps, la vaccination d’AstraZeneca a repris presque partout. Mais les contradictions s’accumulent. Prenez ceci: au départ, seuls les patients de moins de 65 ans étaient éligibles au vaccin dans de nombreux pays, car les données sur les personnes âgées étaient très rares. Après cela, les résultats très positifs venant du Royaume-Uni ont permis d’en faire profiter toutes les catégories d’âge. Mais désormais, suite à ces cas de thrombose, il n’est administré qu’aux personnes de plus de 55 ans dans certains pays, dont la France, car les caillots sanguins concernaient surtout les jeunes.
La confiance est partie
Selon une enquête publiée la semaine dernière par l’Institut Elabe, près de 60% des Français ont déclaré ne pas faire confiance au vaccin AstraZeneca, contre 25% à propos de Pfizer. Les sondages dans d’autres pays montrent une méfiance comparable.
En raison de toutes ces turbulences, certains pays ont même annulé leurs commandes d’AstraZeneca. Par exemple la Nouvelle-Zélande, qui s’est tournée exclusivement vers Pfizer. L’Afrique du Sud a vendu ses doses d’AstraZeneca après que les chercheurs aient conclu qu’il n’offrait qu’une ‘protection minimale’ contre les cas légers à modérés de covid-19 causés par la variante découverte dans le pays.
D’autres pays sont toujours à la recherche de doses d’AstraZeneca: l’Australie et le Canada essaient d’en acheter davantage mais n’y arrivent pas. Et les États-Unis ont eux expédié une partie de leur stock au Canada et au Mexique la semaine dernière. Aux États-Unis, ils s’en sortent déjà bien avec les trois vaccins de plus en plus disponibles: Pfizer-BioNTech, Moderna et Johnson & Johnson. Ils ne veulent pas vraiment du vaccin d’AstraZeneca, qui n’a d’ailleurs pas encore été validé. C’est la dernière polémique en date pour le vaccin qui devait nous mener à un retour à la vie normale: une agence de contrôle américaine a constaté que des données obsolètes figuraient dans les documents transmis. AstraZeneca corrigeait le tir, mais là encore, le mal était fait. La confiance est partie.
Pour aller plus loin :